Боль в суставах – сезонная проблема осени
Пора «бабьего лета» подошла к концу и пожелтевшие листья смывают дожди, устанавливается промозглая погода, становится сыро и холодно…Как часто нам в это время напоминают о себе суставы – иногда ноют, иногда болят, а иногда даже припухают и становится тяжело двигаться.
Да, осенью многие жалуются на боли в суставах. И действительно, повышенная влажность из-за дождей, резкая амплитуда температур и холодный ветер только обостряют заболевания опорно-двигательного аппарата.
Осенью действительно больше пациентов приходят к врачам с жалобами на боли в суставах. Это происходит по различным причинам, индивидуальным для каждого пациента. И терпеть боль, надеясь, что она пройдет со сменой сезона, очень опасно.
Погода и боль
 Болевые ощущения в суставах на самом деле можно связывать с погодными изменениями. Еще Гиппократ отмечал, что у некоторых заболеваний существует сезонный характер. Об этом свидетельствует и китайская медицина. Не случайно проблемы описываемы в современной системе по названием«ревматизм» в древних медицинских системах именуют заболеванием сырости и ветра. Изменения в давлении и температуре действительно способны усиливать болевые ощущения при остеоартрите и ревматоидном артрите. То же относится и к головным болям, зубнымболям, а так же болям и обостряющимся воспалениям в области шрамов, травм и операций, в тех местах, где бывало воспаление ранее: в спине, при невралгии тройничного нерва, фибромиалгии, подагре и фантомных болях в конечностях.
Болевые ощущения в суставах на самом деле можно связывать с погодными изменениями. Еще Гиппократ отмечал, что у некоторых заболеваний существует сезонный характер. Об этом свидетельствует и китайская медицина. Не случайно проблемы описываемы в современной системе по названием«ревматизм» в древних медицинских системах именуют заболеванием сырости и ветра. Изменения в давлении и температуре действительно способны усиливать болевые ощущения при остеоартрите и ревматоидном артрите. То же относится и к головным болям, зубнымболям, а так же болям и обостряющимся воспалениям в области шрамов, травм и операций, в тех местах, где бывало воспаление ранее: в спине, при невралгии тройничного нерва, фибромиалгии, подагре и фантомных болях в конечностях.
Откуда берется боль в суставах?
По одной из теорий, ситуация связана со снижением атмосферного давления, которое иногда предшествует бурям. Эти скачки изменяют и давление в середине сустава. Как говорит профессор Роберта Джэймисона из Гарварда, сустав при таких условиях распухает, давит на окружающие его ткани и нервы, провоцируя боль. Не случайно в большей степени зависят от погоды те, у кого в суставах накапливается жидкость. А накапливается она, как правило, в результате воспаления, пусть и давнего, пусть и не острого, но в его результате может образоваться выпот.
Между тем медики также отмечают, что при резкой смене погоды повышаются риски сердечных приступов, инсультов, неожиданной смерти в среде пациентов с сосудистыми нарушениями. Возможно, ввиду низкой температуры кровь становится более густой и сосуды сужаются. Из-за высокой влажности опухают и лишаются гибкости суставы.
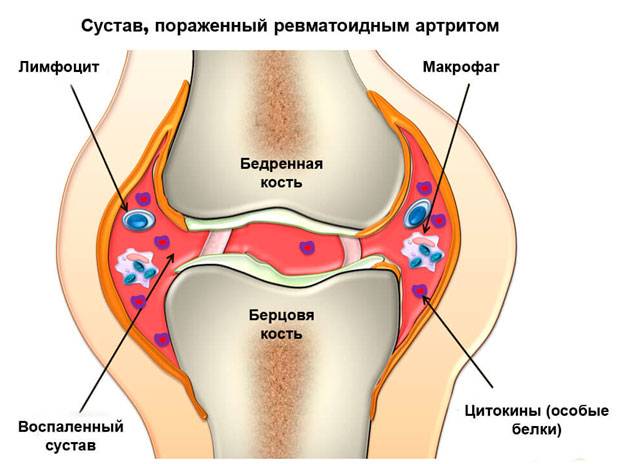
Эти воспалительные заболевания суставов могут быть вызваны различными причинами, да и сам процесс воспаления может протекать с некоторыми отличиями. Такие заболевания, как правило, называются артритами, когда воспаление уже начинает разрушать ткань сустава – артрозами. Этой проблематикой занимается раздел медицины под названием ревматология, а заболевания называются ревматическими.
Боль является самой распространенной причиной, в связи с которой пациент обращается за медицинской помощью к врачу. Известно, что боль сопровождает около 70% всех заболеваний, а распространенность хронической боли среди населения колеблется от 2 до 49%. Одной из наиболее распространенных причин развития болевого синдрома являются ревматические заболевания. С его развитием связывают 30% случаев временной нетрудоспособности и 10% случаев инвалидизации больных.
Ревматические заболевания, сопровождающиеся острой и хронической болью, являются достаточно распространенными. При этом их частота постоянно растет, особенно среди населения развитых стран. Учитывая увеличение числа лиц пожилого и старческого возраста, предполагается, что в течение следующих 20 лет доля лиц с патологией опорно-двигательного аппарата может достичь ⅓ общего числа населения. Поэтому проблема боли, связанной с ревматическими заболеваниями, очень актуальна для общества. Причины появления боли в различных структурах опорно-двигательного аппарата при ревматических заболеваниях разнообразны. Наиболее часто появление боли связано с развитием хронического воспаления в синовиальной оболочке. Боль, сопровождающая поражения суставов и периартикулярных тканей при ревматоидном артрите, остеоартрозе, анкилозирующем спондилите, спондилоартрите, чаще носит хронический характер. В то же время при ряде ревматических заболеваний отмечают приступы острой боли, например при подагрическом артрите.
Боль, сопровождающая ревматические заболевания, представляет собой суммарный результат действия патологических стимулов, обусловленных повреждением тканей опорно-двигательного аппарата и активацией нейрогенных механизмов, что делает целесообразным назначение комплексной терапии. При выборе терапии необходимо учитывать характер боли, психосоциальные параметры и риск возникновения неблагоприятных реакций, связанных с лекарственными средствами.
Много бед один ответ
Часто острый болевой синдром сопровождается выраженной воспалительной реакцией, например, при таких состояниях, как реактивный синовит при остеоартрозе, острая боль в нижней части спины, периартикулярная патология (эпикондилит, бурсит и другое), а также острый подагрический артрит. В этом случае для быстрого купирования боли и воспаления следует отдавать предпочтение нестероидным противовоспалительным препаратам (НПВП), в которых сочетаются быстрое обезболивающее действие и мощный противовоспалительный эффект.
Нестероидные противовоспалительные препараты (НПВП) относятся к числу наиболее востребованных лекарственных препаратов (ЛП) в современное время. Они представляют важное значение для практического здравоохранения, и относятся к наиболее часто применяемым препаратам в повседневной врачебной практике, причем многие из них отпускаются без рецепта врача, то есть легко доступны для населения. Более тридцати миллионов человек в мире ежедневно принимают НПВП, причем 40 % этих пациентов имеют возраст старше 60 лет. По прогнозам, это количество будет только возрастать по мере общего старения населения развитых стран, и, соответственно, увеличения распространенности заболеваний, при которых применяются НПВП. В первую очередь это дегенеративные заболевания опорно-двигательного аппарата и ревматические поражения мягких тканей, что имеет не только медицинское, но и большое социальное значение, так как приводит к длительной потере трудоспособности и инвалидности. По сравнению с другими классами противовоспалительных средств (глюкокортикоиды, препараты базисного лечения) НПВП – наиболее востребованы в клинической практике, их применяют в большинстве случаев воспаления как препараты I ряда. Широкое применение НПВП обусловлено их высокой активностью, быстрым развитием эффекта и относительно высокой безопасностью. Кроме того, эти средства вызывают не только симптоматический болеутоляющий эффект, уменьшают скованность и повышают подвижность суставов, но и оказывают патогенетическое действие, ограничивая повреждающее влияние простаноидных медиаторов воспаления.
Наличие пациентов с коморбидной патологией требует осторожности при назначении НПВП у пациентов с высоким риском сердечно-сосудистой, почечной патологии, заболеваниями печени и желудочно-кишечного тракта. Для повышения эффективности лечения рекомендуется применять препараты класса НПВП в самых низких эффективных дозах и наиболее коротким по длительности курсом.
Основные показания для применения НПВП представляют широкий спектр воспалительных и дегенеративных заболеваний опорно-двигательного аппарата в том числе ревматоидный, псориатический, ювенильный хронический артрит, анкилозирующий спондилит (болезнь Бехтерева), остеоартроз, подагрический артрит, бурсит, тендовагинит. НПВП применяются в основном в качестве симптоматической терапии, уменьшения боли и воспаления на момент использования, что не влияет на прогрессирование заболевания. Анальгетический эффект группы НПВП обусловил их применение при болевом синдроме различной локализации: головная (в том числемигренозная) и зубная боль, люмбаго, ишиалгия, оссалгия, невралгия, миалгия, артралгия, радикулит, болевой синдром при онкологических заболеваниях, посттравматический и послеоперационный болевой синдром, сопровождающийся воспалением. НПВП применяют при инфекционно-воспалительных заболеваниях ЛОР органов с выраженным болевым синдромом (в составе комплексной терапии): фарингит, тонзиллит, отит, лихорадочный синдром при «простудных» заболеваниях и гриппе.
Одной из наиболее распространенных форм заболеваний опорно-двигательного аппарата, наряду с такими заболеваниями как рак, туберкулез, сахарный диабет, патология сердечно-сосудистой системы, одно из первых мест среди причин потери трудоспособности и инвалидности занимает остеоартроз (ОА). Наиболее характерными симптомами ОА являются постоянные боли в области суставов, что предполагает назначение НПВП с высоким анальгетическим индексом и хорошей переносимостью.
Важнейшим вопросом современной фармакотерапии является не только эффективность, но и безопасностьлекарств. Одним из наиболее частых и распространенных рисков применения НПВП является возможное поражение желудочно-кишечного тракта (ЖКТ). Выделяют большую группу заболеваний, при которых нарушение равновесия между факторами агрессии желудочного содержимого и защитными факторами слизистой оболочки желудка и двенадцатиперстной кишки, являются классическим представлением о патогенезе эрозивно-язвенного поражения ЖКТ на всем его протяжении. Доказано, что длительный прием некоторых групп лекарственных препаратов является важным повреждающим фактором слизистой оболочки желудка и двенадцатиперстной кишки. Так, НПВП (ацетилсалициловая кислота, индометацин, кеторолак, диклофенак, и другое) и глюкокортикостероидные препараты способствуют угнетению защитных факторов, первые за счет подавления синтеза простагландинов, вторые за счет влияния на процессы микроциркуляции, регенерации и стимуляции секреции соляной кислоты и пепсина. Поэтому актуальной задачей рациональной фармакотерапии пациентов, у которых одновременно присутствует несколько заболеваний, в том числе сочетания заболеваний опорно-двигательного аппарата и желудочно-кишечного тракта, является возможность предотвращения риска развития осложнений при совместном применении препаратов класса НПВП.
Механизм действия НПВП достаточно хорошо изучен (Рис.1). Широкое применение НПВП объясняется их универсальным спектром действия. Они обладают противовоспалительным, анальгезирующим и жаропонижающим эффектами и приносят облегчение больным с соответствующими симптомами, которые отмечаются при многих заболеваниях.
В первую очередь, благодаря их анальгетической активности, они одновременно составляют и группу ненаркотических (неопиатных) анальгетиков. Важно, что начав лечение с НПВП, больные ревматическими заболеваниями очень редко (не более чем в 10 % случаев) переходят на прием простых анальгетиков.
Болевой синдром – может быть отдельной патологией
Едва ли в клинической медицине можно отметить другой, столь частый и разнообразный по характеру проявлений и причинам феномен, как боль. Изначально она может формироваться как важная защитная биологическая реакция организма. Однако, сильная, или длительно существующая боль сама формирует очаги патологического возбуждения, усиливающие функционально-морфологические изменения в органах и костно-мышечных образованиях. Важно подчеркнуть, что острая боль – это симптом, а хроническая боль может стать, по существу, самостоятельным заболеванием.
НПВП могут рассматриваться как патогенетические средства, что значительно расширяет и трансформирует представление о препаратах этой группы не только в качестве средств симптоматической терапии.Действие анальгетиков направлено на предупреждение и уменьшение активации первичных афферентов «альгетиками» и подавление передачи болевого импульса на сегментарном и супрасегментарном уровнях. Иногда целесообразно назначить профилактически,для защиты пациента от действия операционной травмы НПВП до операции. Механизм данного эффекта связан с предотвращением центральной гиперсенсибилизации нейронов задних рогов спинного мозга, воздействием НПВП на периферические и центральные механизмы появления и развития острой боли, тем самым предупреждая патологические нейропластические изменения в спинном мозге. Это предусматривает исключение вероятности перехода физиологической боли в патологическую (нейропатическую).
Сегодня арсенал НПВП достаточно широк. Препараты этой группы традиционно разделяют по их химическому строению. Однако данная классификация не характеризует свойства различных групп средств. Для понимания особенностей действия препаратов и правильного применения их в клинической практике важно знать различия в механизме действия тех или иных НПВП и, соответственно, классифицировать их по механизму действия.
По современным представлениям, ключевой и наиболее общий механизм противовоспалительного действия НПВП – угнетение ими биосинтеза простагландинов (ПГ) из арахидоновой кислоты.
В сложном комплексе реакций, составляющих воспалительный процесс, участвуют многочисленные биологически активные вещества, которые определяются как медиаторы воспаления. В их число входят белки и полипептиды (кинины и калликреины), лейкоцитарные факторы (факторы хемотаксиса, интерлейкины,антикейлоны и др.), белки системы комплимента;биогенные амины (гистамин и серотонин) и продукты метаболизма арахидоновой кислоты – эйкозаноиды(простагландины, простациклин, тромбоксаны) и лейкотриены.
Классификация НПВП
 Общепринятой считается классификация НПВП по механизму действия.
Общепринятой считается классификация НПВП по механизму действия.
- Так, к селективным ингибиторам ЦОГ-1 относится ацетилсалициловая кислота в низких дозах (0,1–0,2 в сутки).
- Неселективными ингибиторами ЦОГ-1 и ЦОГ-2 (нНПВП) считаются:ацетилсалициловая кислота в высоких дозах (1,0–3,0 в сутки и более); фенилбутазон; ибупрофен; кетопрофен; напроксен; нифлумовая кислота; пироксикам; лорноксикам; диклофенак; ацеклофенак; индометацин и ряд других НПВП.
- Селективные ингибиторы ЦОГ-2 (сНПВП): мелоксикам; нимесулид.
- Высокоселективные ингибиторы ЦОГ-2 (сНПВП): целекоксиб; эторикоксиб.
- Селективные ингибиторы ЦОГ-3: ацетаминофен; метамизол натрия.
По современным представлениям, ключевой и наиболее общий механизм противовоспалительного действия НПВП – угнетение ими биосинтеза простагландинов из арахидоновой кислоты (Рис.1).
Еще в 1970-х гг. была высказана версия о существовании разных типов ЦОГ, а затем и открытие двух изоформ ЦОГ: ЦОГ–1 и ЦОГ–2. ЦОГ-1 постоянно экспрессируется и функционирует в тканях и органах и участвует преимущественно в регуляции физиологических процессов. Экспрессия ЦОГ-2 (уровень активности которой в физиологических условиях весьма низкий) индуцируется цитокинами при повреждении или воспалении тканей, с ее активностью связывают синтез флогогенных ПГ.
Синтез этих изоферментов регулируется различными генами, они отличаются по молекулярной структуре и обладают разной (хотя и частично перекрещивающейся) функциональной активностью, отражающей их различную роль в реализации «физиологических» и «патологических» эффектов ПГ. Открытие изоформ ЦОГ имело не только важное теоретическое, но и большое практическое значение. Во-первых, оно позволило объяснить причины эффективности и токсичности (прежде всего гастроэнтерологической) «стандартных» НПВП, которая в первую очередь связана с подавлением активности обеих изоформ ЦОГ. Во-вторых, предоставило экспериментальное обоснование для разработки «новых» НПВП, так называемых ингибиторов (селективных или специфических) ЦОГ–2, обладающих более низкой гастроэнтерологической токсичностью, чем «стандартные» НПВП. В процессе этих исследований был частично расшифрован механизм действия «простого» анальгетика парацетамола, точкой приложения которого оказалась еще одна изоформа ЦОГ (ЦОГ–3), преимущественно локализующаяся в клетках коры головного мозга. Это позволило классифицировать ненаркотические анальгетики не по их химическим свойствам, а по фармакологическим (ЦОГ–зависимым) механизмам действия. Синтез более новых препаратов (в т.ч. коксибов) базируется на данных о структурной и функциональной гетерогенности ЦОГ.
Одним из наиболее известных и широко распространенных препаратов является диклофенак. Сегодня диклофенакпризнан золотым стандартом в ревматологии. Это лекарственное средство с огромным опытом применения, механизмы анальгезирующего и противовоспалительного действия которого достаточно хорошо изучены, что позволяет рекомендовать его при широком спектре различных патологических состояний, связанных с наличием болевого синдрома и воспаления. Диклофенак является производным фенилуксусной кислоты (2-[2,6-дихлоранилино]фенилуксусная кислота), обладающим обезболивающим, противовоспалительным и жаропонижающим эффектом. Среди наиболее эффективных НПВП диклофенак характеризуется хорошим сочетанием выраженного противовоспалительного и болеутоляющего действия с приемлемой переносимостью. Анальгезирующий эффект диклофенакаобусловлен прежде всего ингибированием активности циклооксигеназы (ЦОГ) – фермента, регулирующего превращение арахидоновой кислоты в простагландины, которые являются медиаторами воспаления, задействованы в формировании болевого синдрома и повышении температуры тела. ЦОГ имеет две изоформы, отличающиеся по ряду параметров, в частности по локализации в тканях, функциональной роли. ЦОГ-1 (конститутивная) в различных количествах присутствует практически во всех тканях и регулирует образование физиологических простагландинов (Рис.1). ЦОГ-2 в норме практически не определяется, но ее уровень возрастает в десятки и сотни раз при развитии воспалительного процесса. Диклофенак ингибирует оба изофермента ЦОГ, в большей степени – ЦОГ-2 (Рис.1).
Широко известной является высокая эффективность диклофенака в купировании хронической боли. При этом результаты многих клинических исследований доказывают его эффективность и при острой боли, в том числе при приступе подагрического артрита, боли в пояснице при остеохондрозе, боли после оперативного вмешательства. В этом случае актуальны лекарственные формы диклофенака для внутримышечного введения. Известно, что при внутримышечном введении анальгезирующий эффект диклофенака наступает через 15–30 мин. Именно по этой причине инъекционные формы диклофенака хорошо подходят для купирования острой боли. При этом с целью повышения эффективности и удобства применения диклофенака постоянно продолжают разрабатываться его новые формы выпуска, в том числе в комбинации с другими анальгетиками.
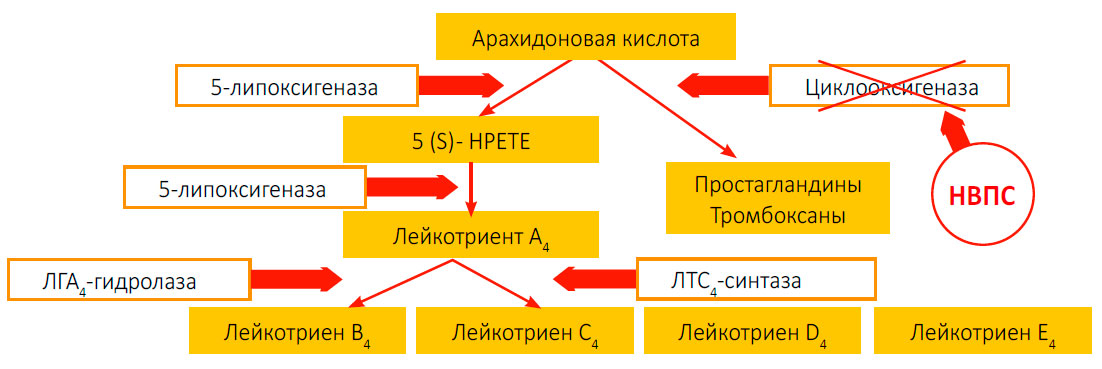
Рис.1. Механизм действия НПВП
ДИКЛОФЕНАК-ВИОЛА симптом-модифицирующий препарат быстрого действия
 Высокий профиль безопасности, новая форма лекарства, способная ускорить противовоспалительное действие и уменьшить побочные эффекты — все это делает ДИКЛОФЕНАК-ВИОЛА одним из наиболее современных и рекомендуемых в лечении болевого синдрома в ревматологической практике. Патогенетическое действие лекарственного средства позволяет не только останавливать воспалительный процесс, но и восстанавливать поврежденные воспалительными медиаторами ткани суставов. Целесообразность применения ДИКЛОФЕНАК-ВИОЛА в комплексной терапии больных определяется его позитивным действием на метаболизм гиалинового хряща, хотя ряд НПВП в подавляющем большинстве случаев угнетает его метаболизм и, соответственно, может приводить к прогрессированию заболевания.
Высокий профиль безопасности, новая форма лекарства, способная ускорить противовоспалительное действие и уменьшить побочные эффекты — все это делает ДИКЛОФЕНАК-ВИОЛА одним из наиболее современных и рекомендуемых в лечении болевого синдрома в ревматологической практике. Патогенетическое действие лекарственного средства позволяет не только останавливать воспалительный процесс, но и восстанавливать поврежденные воспалительными медиаторами ткани суставов. Целесообразность применения ДИКЛОФЕНАК-ВИОЛА в комплексной терапии больных определяется его позитивным действием на метаболизм гиалинового хряща, хотя ряд НПВП в подавляющем большинстве случаев угнетает его метаболизм и, соответственно, может приводить к прогрессированию заболевания.
Представлены данные американских и европейских ученых о влиянии НПВП на метаболизм суставного хряща. Они были получены в основном в эксперименте на модели культуры ткани суставного хряща, поэтому к этим результатам следует относиться с некоторой оговоркой. Но не вызывает сомнений то, что действие НПВП на метаболические процессы в хондроцитах тесно связано с их метаболической активностью, протестированной дозой исследуемого препарата, возрастом донора, стадией заболевания и степенью повреждения хряща. Что касается ДИКЛОФЕНАКА, то, в отличие от некоторых традиционных НПВП, он не оказывает значительного повреждающего действия на суставной хрящ.
Хондротропное влияние ДИКЛОФЕНАКА активно изучалось как в эксперименте, так и в клинике. Исследования in vitro и in vivo показали, что он повышает синтез протеогликанов в эксплантанте остеоартрозного хряща, полученного у больных с различной степенью тяжести остеоартроза, подавляет продукцию NO, воздействует на свободные радикалы, тормозит апоптоз хондроцитов, может нейтрализовать действие ММП, ингибирует деградацию аггрекана. Кроме того, он ингибирует экспрессию провоспалительных цитокинов, прежде всего интерлейкина 1. Эти данные позволяют рассматривать ДИКЛОФЕНАК-ВИОЛА в качестве препарата, обладающего определенными хондропротективными свойствами.
При изучении НПВП большое внимание уделяется их переносимости и безопасности. Во многих исследованиях воспалительных заболеваний суставов продемонстрирована более высокая безопасность ДИКЛОФЕНАКА по сравнению с другими НПВП.
Заключение
Рациональная фармакотерапия пациентов с коморбидной патологией, страдающих как заболеваниями сердечно-сосудистой системы, желудочно-кишечного тракта, так и патологией опорно-двигательного аппарата, необходимость проведения симптоматической терапии болевого и воспалительного синдромов должна проводиться с учетом персонализированного подхода к пациенту и рациональном выборе лекарственных средств.
Наиболее отчетливо это проявляется при приеме НПВП.
Рациональное назначение НПВП позволит улучшить прогноз заболевания, повысить приверженность больного к проводимой терапии и качество жизни пациента. Таким образом, ДИКЛОФЕНАК-ВИОЛА оказывает отчетливое противовоспалительное и анальгетическое действие и отличается хорошей переносимостью, что делает возможным его широкое использование в терапии ревматоидных заболеваний. Особенно интересным представляется влияние ДИКЛОФЕНАК-ВИОЛА на гиалиновый хрящ, что позволяет рассматривать его в качестве потенциального хондропротективного препарата.
![]() Давыдова Т.В., кандидат медицинских наук, иммунолог, научный сотрудник лаборатории и клинического отдела иммунофармакологии ГУ «Институт микробиологии и иммунологии им. И.И. Мечникова Национальной академии медицинских наук Украины»
Давыдова Т.В., кандидат медицинских наук, иммунолог, научный сотрудник лаборатории и клинического отдела иммунофармакологии ГУ «Институт микробиологии и иммунологии им. И.И. Мечникова Национальной академии медицинских наук Украины»
 07-июн-2026
07-июн-2026