Як захистити себе від бактеріальних інфекцій у сезон застуд

Погодні умови з різким похолоданням, дощовою сльотою — одна з провідних ознак початку сезону гострих респіраторних інфекцій, які викликаються як вірусами, так і бактеріями.
У багатьох людей під час зміни сезонів активізуються вогнища хронічних бактеріальних інфекцій, які довгий час дрімали в носоглотці. Це стрептококи, стафілококи і інші патогенні та умовно-патогенні мікроорганізми, які можуть викликати запалення. Також причетні до цієї проблеми і грибки. Грибкові інфекції — часті мешканці носоглотки дорослих і дітей з хронічною патологією верхніх дихальних шляхів.
Навіть після одноразового інфікування в переважній більшості випадків інфекційний агент при лікуванні і, тим більше, без нього повністю не зникає зі слизових оболонок носоглотки і поверхні мигдалин. В результаті лікування та/або під впливом нашого власного імунітету гостре запалення минає, більшість мікроорганізмів гине, але невелика їх частина може залишитися і трансформуватися в співтовариства, так звані «біоплівки», стати невидимими для імунітету і застосувати багато інших хитрощів для власного порятунку. І чекати. Чекати слушної нагоди для розвитку нового запального процесу — своєрідного «революційного повстання». І з настанням осінньо-зимового періоду цей сприятливий випадок якраз видається. І повторюючись з разу в раз — мікроорганізми стають все стійкішими, а нам ставлять діагноз — хронічний фарингіт, хронічний риніт, ларингіт і так далі. Таким чином, кожен сезон застуд стає для нас справжнім викликом.
Місцевий імунітет страждає від наявності постійного підгострого запалення. Слизові стають все більш сприйнятливими до нових інфекцій і все більш беззахисними перед старими. Згодом це може позначитися і на інших органах і системах, що проявляється аутоімунним ураженням сполучної тканини і інших органів.
На частку гострих респіраторних інфекцій припадає понад 90 % всіх захворювань дихальної системи у дорослих і дітей. Повторні вірусні інфекції призводять до пошкодження циліарного епітелію слизової оболонки дихальної системи, порушення цілісності власної мікробної біоплівки, вивільнення великої кількості активних форм персистуючих мікробів.
Розвиваються дисбіотичні порушення мікрофлори носоглотки, тих природних «хороших» бактерій, які, перебуваючи в достатній кількості, перешкоджають впровадженню зовнішніх інфекційних агентів. Ці зміни мікробіома носоглотки зберігаються після перенесеного ГРЗ протягом декількох місяців. Зі збільшенням числа загострень зростає частота і спектр культур, що висіваються. Вторинні за своєю природою зрушення нормальної флори можуть брати на себе патогенетичне лідерство, ініціюючи розвиток повторних респіраторних захворювань.
Тому, звичайно ж, найбільш схильні до простудних захворювань люди з хронічними назофарингітами і бронхітами, алергіки і особи, які працюють професійно в контакті з речовинами, що подразнюють дихальні шляхи (пил, хімічні речовини, біологічні подразники).
В основному, хронічний фарингіт формується як результат тривалого місцевого впливу на слизову глотки. Спочатку гострий процес, який не усувається, тривало подразнює слизові, що в кінцевому результаті призводить до хронізації процесу. Також сприяють формуванню хронічного процесу наявність інших проблем — тонзиліти, синусити, постійний нежить або запалення аденоїдів. При цьому слиз, який стікає в носоглотку, подразнює її стінки і призводить до запалення і поширення інфекційних агентів. При наявності постійного нежитю, хронічний фарингіт може бути спровокований невгамовним застосуванням судинозвужувальних засобів, які активно стікають в глотку. Наявність аденоїдів нерідко тягне за собою сам фарингіт, через наявність постназального синдрому, він же синдром постназального затікання — запальний процес в порожнині носа, носових пазухах або носоглотці, при якому слиз стікає в нижні відділи дихальних шляхів по задній стінці.
До розвитку фарингіту може призводити і вплив зовнішніх несприятливих чинників — підвищена запиленість повітря, гаряче повітря на виробництві або занадто пересушене в сезон опалення повітря в домашніх умовах, наявність в повітрі хімічних речовин. Нерідко страждають від хронічного фарингіту курці і люди, які вживають алкоголь (це викликано негативним впливом даних речовин на слизові носоглотки).

Мікробний пейзаж носа і горла у часто хворіючих людей зі зниженням місцевої захисної функції часто представлений монокультурою дифтероїдів — грампозитивних паличок групи Corynebacterium, різними видами грампозитивних коків сімейства Micrococcaceae: Staphylococcus saprophyticus, Staphylococcus aureus, Staphylococcus epidermidis, а також Streptococcus haemolyticus, Streptococcus viridens або асоціаціями бактерій групи Corynebacterium і сімейства Micrococcaceae. Зазвичай це відбувається на тлі зниження кількості мікроорганізмів групи Lactobacter, при таких умовах може збільшуватися присутність грибів роду Candida, а в особливо складних ситуаціях в носоглотці з’являються бактерії кишкової групи, що свідчить про значне зниження імунітету.
У фахівців є навіть поняття дисбіоз слизової оболонки носа і горла різних ступенів.
У категорії осіб з частими рекурентними захворюваннями дихальних шляхів нерідко виявляються ознаки імунного дисбалансу та недостатності резервних можливостей імунітету. Наслідками частих респіраторних захворювань можуть бути порушення функціональної активності імунної системи і формування хронічних запальних процесів в органах дихання [1, 3].
В останні роки для лікування і профілактики респіраторних захворювань активно використовуються імунокоректори бактеріального походження, перш за все бактеріальні лізати, що викликають формування селективної імунної відповіді проти найбільш поширених бактеріальних збудників, також активують неспецифічні механізми вродженого імунітету, які допомагають боротися як з бактеріями, так і з вірусами. Бактеріальні лізати були розроблені з метою запобігання інфекційних захворюваннь верхніх і нижніх дихальних шляхів і являють собою суміш антигенів, отриманих з різних інактивованих бактерій, що представляють собою патоген-асоційований молекулярний агент, що приводить до запуску каскаду місцевих імунних реакцій. Лізати бактерій мають подвійне призначення: специфічне (вакциноподібне) і неспецифічне (імуномодулююче) [4].
Секреторний імуноглобулін А як фактор місцевого захисту слизових оболонок дихальних шляхів: причини його зниження і корекції
 Особливо важливим в цьому випадку є фактори первинного захисту, які присутні на бар’єрних покривах нашого організму: шкірі і слизових — показники вродженого імунітету. Одним з основних є імуноглобулін А.
Особливо важливим в цьому випадку є фактори первинного захисту, які присутні на бар’єрних покривах нашого організму: шкірі і слизових — показники вродженого імунітету. Одним з основних є імуноглобулін А.
Дихальна система людини — це вхідні ворота для речовин, що забруднюють навколишнє середовище, і збудників різних хвороб, тому стан імунного захисту в цьому органі має бути вирішальним фактором в елімінації несприятливого компонента при вдиханні. Стан місцевого імунітету слизової оболонки залежить від її цілісності, вмісту імуноглобулінів А, G і М, стану лімфоїдної тканини.
Імуноглобуліни — це білки, які відповідають за інактивацію і знищення інфекційних агентів. Одним з імуноглобулінів, що відіграє важливу роль в зfхисті респіраторного тракту, є секреторний імуноглобулін А (sIgA). Цей захисний імуноглобулін є подвійною білковою молекулою, форма і будова якої оберігає його від руйнування і дозволяє бути активним довго навіть під впливом різних несприятливих факторів. Однак живе він всього 5 днів. Тому для його постійного поповнення в організмі щодня відбувається диференціювання В-лімфоцитів у плазматичні клітини, так як саме вони синтезують sIgA. Для запуску даного процесу навколишні клітини продукують цитокіни — біологічно активні речовини-стимулятори, які сприяють цій трансформації і початку синтезу sIgA.
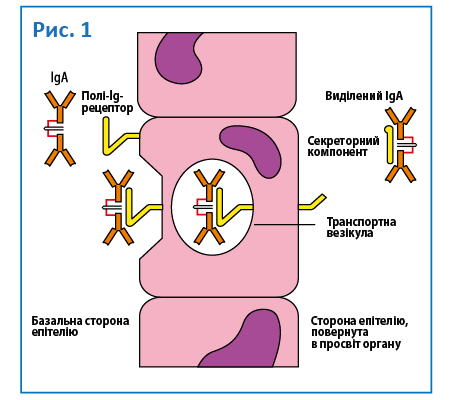
До того ж епітеліальні клітини продукують глікопротеїн, що називається секреторним компонентом, який є основною ланкою в місцевій імунній системі. Він забезпечує стабільність sIgA і транспортує IgA і IgM до поверхонь нашого тіла, тобто слизових і шкірі, які є першим бар’єром з зовнішнім середовищем і інфекціями. Останні дослідження припустили можливу роль епітеліальних клітин в антигенній презентації. Дендритні клітини, специфічні клітини-розвідники, які виявляють і передають інформацію про «ворога», знаходяться в епітелії дихальних шляхів, можуть безпосередньо надавати антигени В-лімфоцитів і, таким чином, стимулювати їх до диференціювання, тобто перетворення і специфікації в необхідні для захисту клітини за допомогою цитокінів і до синтезу sIgA (рис.1) [5].
Трохи відвернемося від серйозних імунологічних термінів, глибоких механізмів формування захисту слизових оболонок і спробуємо зрозуміти, що ж може допомогти нам сформувати надійний захист наших дихальних шляхів.
Отже, щоб sIgA синтезувався в достатній кількості, потрібно, щоб імунітет у цілому весь час був насторожі, був натренований швидко і ефективно реагувати на інфекції і запалення. І найбільш дієвим способом в цій стимуляції є «гарт» імунітету.
Як зробити імунний захист слизових сильнішим?
Одним із способів профілактики та лікування респіраторних інфекцій є застосування лізатів бактерій.
Що це за препарати? Їх механізм дії заснований на активації імунної відповіді на найпоширеніші мікроорганізми, що викликають запалення органів респіраторної системи.
Лізати представляють собою частинки клітин бактерій, отримані в результаті їх руйнування. У відповідь на їх введення запускається каскад імунологічних реакцій, що в результаті допомагає організму сформувати імунітет і впорається із захворюванням. Бактеріальні лізати не викликають дисбактеріоз, що особливо важливо при лікуванні дітей.
З’явилися препарати, що містять лізати бактерій, ще в 70-х роках XX століття, однак і зараз вони продовжують залучати інтерес багатьох фахівців різних галузей медицини. Їх призначають для профілактики і лікування інфекцій, частих запалень органів дихання, а також шкіри і органів сечостатевої системи.
Механізм їх дії пов’язаний, з одного боку, з виробленням специфічного IgA і фіксацією його на слизових, а з іншого, — з активацією імунної системи (Т-, В-клітини, макрофаги, дендритні клітини).
В то же час, активація макрофагальної ланки, цитотоксичних Т-лімфоцитів призводить до знищення інфікованих клітин і інфекційних агентів. Специфічні і неспецифічні механізми дії бактеріальних імуномодуляторів визначають їх ефект не тільки проти бактерій, лізати яких входять до складу препаратів, а й проти інших збудників респіраторних інфекцій, що можна простежити за частотою ГРВІ в групі часто хворіючих дітей [3].
Механічний лізис здійснюється шляхом збільшення тиску на стінку інактивованої бактерії, що зберігає крупнодисперсні антигени, в той час, як хімічний лізис відбувається із застосуванням хімічних агентів для руйнівного впливу на бактеріальні агенти, що може привести до денатурації білків і, отже — антигенів. Таким чином, препарат, отриманий методом механічного лізису, володіє сильнішою імуногенністю.
Взаємодія бактеріальних антигенів зі спеціальними TLR-рецепторами на поверхні дендритних клітин призводить до дозрівання, активації дендритних клітин і їх міграції в лімфатичні вузли. Дендритні клітини презентують (показують мітки «ворожих агентів») антигени Т і В-клітинам, що супроводжується синтезом біологічно активних імунологічних речовин — цитокінів, диференціюванням-трансформацією Т-хелперів для захисту саме від певних інфекційних агентів. Надалі відбувається перетворення В-клітин в плазматичні клітини, які синтезують специфічні імуноглобуліни, особливо IgA і sIgA, які і захищають слизові оболонки.
Антитіла забезпечують процес опсонізації (виявлення і поглинання) патогенних мікроорганізмів, що робить можливим захоплення і знищення патогенних мікроорганізмів фагоцитами. Даний механізм дії дозволяє знизити частоту, тривалість і тяжкість інфекційних захворювань дихальної системи. Опсонізація пов’язана з розпізнаванням специфічних мембранних антитіл, що покривають патоген. Фагоцити мають специфічні рецептори для IgG- і IgA-антитіл, що дозволяє фагоцитувати — захоплювати і «поїдати», патогени, покриті антитілами, і знищувати їх за допомогою ферментів фагосом. Гострота запалення і виділення специфічних IgM-антитіл, синтезованих на ранньому етапі імунної відповіді, в комплексі з патогеном активують компоненти комплементу С3b і C4b (спеціального білка-помічника, який підсилює імунну відповідь), покращують виявлення бактерій та інших патогенів. Фагоцити мають рецептори для цих компонентів комплементу, крім того, компонент С5 здатний активувати і посилювати фагоцитоз, що приводить до знищення патогена [11].
Препарат БРОНХО-МУНАЛ, виробництва компанії Sandoz, відноситься до групи механічних лізатів, і таким чином забезпечує збереження структури антигенів бактеріальної стінки, підвищує їх імуногенність. Стимуляція синтезу sIgA забезпечує більш повноцінне виявлення і поглинання агресивних бактерій, а також в цілому робить слизові більш стійкими до дії і впровадження інших збудників [10].
Механізми дії і ефективність системних і топічних імунотропних засобів різні. Недостатній вплив місцевих імуномодуляторів може бути пов’язаний з коротким часом контакту і недостатнім захопленням препарату зі слизових оболонок внаслідок постійного змивання слиною області ротоглоткового сегменту.

Бактеріальні лізати мають ряд специфічних властивостей на всіх стадіях імунної відповіді, завдяки яким ефективність їх застосування набагато вище. Механізм дії полягає в стимуляції процесів фагоцитозу і презентації антигену, посилення продукції протизапальних цитокінів (ІЛ-4, ІЛ-10, ТРФ), розвитку ад’ювантного ефекту. При цьому цей механізм є більш природним і фізіологічним, так як бактеріальні лізати стимулюють власні місцеві реакції організму на вплив антигену і не викликають непотрібних додаткових ефектів. Поряд з продукцією специфічних антитіл до складових препарату, вони також стимулюють неспецифічний імунітет — підвищується продукція секреторних IgA, інтерлейкіну-1 і α-інтерферону, цитокінів, NK-клітин, клітин макрофагально-фагоцитарної системи та інших систем [6, 7].
БРОНХО-МУНАЛ формує захисний імунологічний бар’єр на слизових оболонках дихальних шляхів, активуючи власний імунітет. В результаті тривалість захворювання скорочується, а профілактичний ефект зберігається протягом декількох місяців. БРОНХО-МУНАЛ можна застосовувати і в розпал захворювання. Крім того, при застосуванні препарату знижується ризик розвитку різних ускладнень ГРЗ. БРОНХО-МУНАЛ має високий профіль безпеки: його застосування можливе з 12-річного віку, БРОНХО-МУНАЛ П, що містить меншу кількість ліофілізату може призначатися вже з 6 місяців.
Препарати БРОНХО-МУНАЛ® і БРОНХО-МУНАЛ® П містять ліофілізований лізат найбільш розповсюджених збудників гострих респіраторних захворювань: Streptococcus pneumoniae, Haemophilus influenzae, Klebseiella pneumoniae, Klebseiella ozaenae, Staphylococcus aureus, Streptococcus viridans, Streptococcus pyogenes, Moraxella catarrhallis.
Кожна капсула БРОНХО-МУНАЛ® містить 7 мг ліофілізату, а БРОНХО-МУНАЛ® П — 3,5 мг [10, 12].
Призначення бактеріальних лізатів, на прикладі дослідження з ОМ-85, для профілактики рецидивів хронічного бронхіту знижує частоту і тяжкість рецидивів, зменшує частоту госпіталізацій і тривалість перебування на лікарняному листі. У дітей з хронічним риносинуситом відзначено зниження частоти рецидивів і тяжкості симптомів [9].
Бактеріальні лізати можна призначати з профілактичною метою, починати прийом можна навіть в гострий період захворювання у комбінації з іншими методами лікування.
Для профілактики інфекційних захворювань дихальних шляхів БРОНХО-МУНАЛ® призначають по 1 капсулі на день натщесерце протягом 10 послідовних днів у місяць, 3 місяці поспіль. Якщо пацієнт забув прийняти препарат, слід прийняти його наступного ранку. Вміст капсули БРОНХО-МУНАЛ® П можна розмішати у відповідному напої (воді, фруктовому соку, молоці).
Таким чином, БРОНХО-МУНАЛ® впливає на різні ланки імунної системи, стимулює клітинний і гуморальний імунітет, що у дорослих і дітей з частими повторними захворюваннями призводить до зменшення частоти і тяжкості інфекцій, зниження необхідності застосування антибіотиків. БРОНХО-МУНАЛ® ефективний в лікуванні і профілактиці інфекційних захворювань як верхніх, так і нижніх дихальних шляхів.
При виборі засобів для лікування та профілактики ГРВІ пам’ятайте, що багато чого залежить і від вас: ГРВІ не можна запускати, це захворювання важливо лікувати і робити це вчасно, щоб одужання настало швидко, а хвороба пройшла без ускладнень.
Інформація для спеціалістів охорони здоров’я 4-49-БРМ-ОТС-0221
Література:
- Комплексный подход к лечению и профилактике острых респираторных инфекций у детей: Практическое руководство для врачей / Под ред. проф. Н.А. Геппе, проф. А.Б. Малахова. М., 2012. — 47 с.
- Simon H. B. Bacterial infections of the upper respiratory tract // ACP Medicine. 2010.
- Самсыгина Г.А. Часто болеющие дети: проблемы патогенеза, диагностики и терапии // Педиатрия. — 2005. — № 1. — с. 66–74.
- Иванова Н. А. Системные бактериальные лизаты: механизм действия и показания к применению // Consilium Medicum. Педиатрия. 2015; 02: 29–32.
- Гуров А.В., Мужичкова А.В., Набиева Т.Т. Клинико-иммунологическое обоснование применения бактериальных лизатов в оториноларингологии // Вестник оториноларингологии. — 2012. — № 77(2):102-107.
- Малахов А.Б., Колосова Н.Г., Хабибуллина Е.В. Бактериальные лизаты в программах профилактики респираторных инфекций у детей // Практическая пульмонология. — 2015. — № 4. — с. 16–19.
- Del-Rio-Navarro B. E., Espinosa Rosales F., Flenady V., Sienra Monge J. J. L. Immunostimulants for preventing respiratory tract infection in children // Cochrane Database Syst Rev. 2996; 4: CD004974.
- SteurerStey C., Lagler L., Straub D. A., Steurer J., Bachmann L. M. Oral purified bacterial extracts in acute respiratory tract infections in childhood: a systematic quantitative review // Eur. J. Pediatr. 2007. Vol. 166, № 4. P. 365–376.
- Sprenkle M.D., Niewoehner D.E., MacDonald R., Rutks I., Wilt T. J. Clinical efficacy of OM85 BV in COPD and chronic bronchitis: a systematic review // COPD. 2005. Vol. 2, № 1. P. 167–175.
- Інструкція для медичного застосування лікарського засобу БРОНХО-МУНАЛ® (BRONCHO-MUNAL®). Реєстраційне посвідчення: UA/14314/01/01.
- Mellioli J. Deciders in pulmonology. (Принятие решений в пульмонологии) // Giorn. It. Mal. tor. 2002. Vol. 56, 4, P. 245–268. GIMT 56.
![]() Тетяна Давидова,
Тетяна Давидова,
кандидат медичних наук, лікар-імунолог, науковий співробітник
лабораторії та клінічного відділу молекулярної імунофармакології ДУ
«Інститут мікробіології та імунології ім. І. І. Мечникова
Національної медичної академії наук України»

 05-июн-2026
05-июн-2026
