Травинор и Дорзитим®— Ваш контроль над глаукомой!
Глаукома — это хроническая прогрессирующая мультифакторная офтальмологическая патология, характеризующаяся постоянным или периодическим повышением внутриглазного давления (ВГД), вызванная нарушением циркуляции внутриглазной жидкости и возникающая на фоне дистрофических изменений дренажной системы глаза и решетчатой пластинки склеры (Курилина Е.И., 2009, Gabor Hollo, 2009). Результатом повышенного внутриглазного давления является постепенное развитие характерных для глаукомы нарушений зрительных функций, глаукоматозной экскавации с последующей атрофией зрительного нерва (Войцеховский А.В., 2006; Jamie D., Croxtall J. Scott, 2009).
Основные механизмы развития глаукомы
Глаукома характеризуется патологической дегенерацией ганглиозных клеток сетчатки, структурными повреждениями в головке зрительного нерва. В результате гибели нейронов при глаукоме возникают дефект слоя нервных волокон сетчатки, истончение нейроретинального ободка с экскавацией диска зрительного нерва и необратимой потерей его волокон. Дегенерация нейронов при глаукоме не ограничивается сетчаткой, изменяются также нейроны латерального коленчатого тела и зрительной коры. 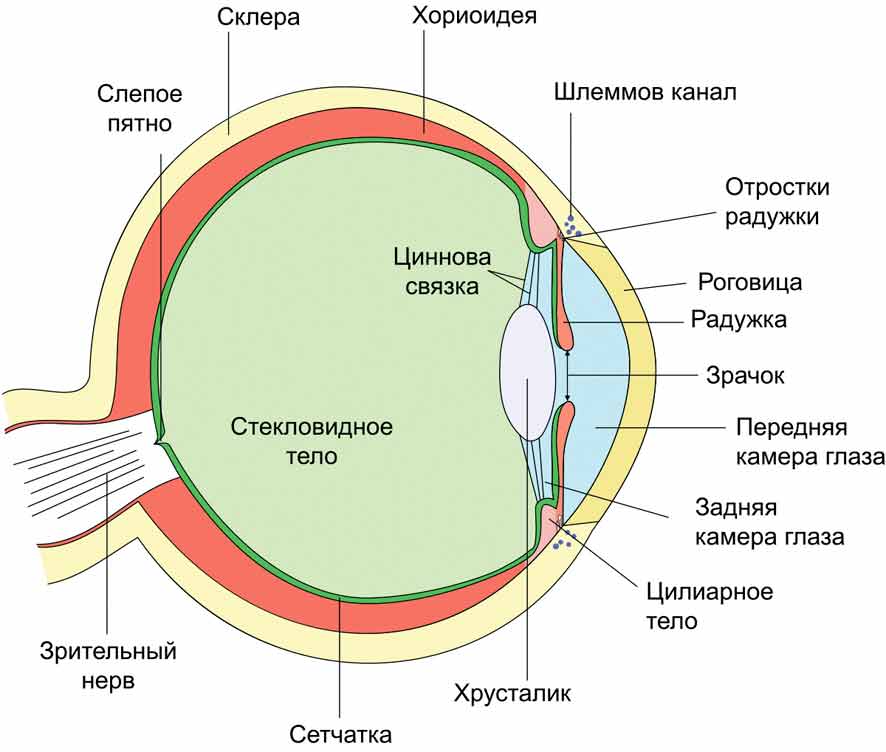 Патологические явления усугубляются изменениями окружающих тканей, что вызвано активацией глиальных клеток, прежде всего астроцитов. Они начинают вырабатывать различные патологические субстанции, например, эндотелин, суживающий сосуды, а также матриксные металлопротеиназы, что приводит к исчезновению последнего и замещению его другим субстратом. Это явление получило название «ремоделирование тканей». Именно данный процесс лежит в основе изменений решетчатой мембраны склеры при глаукоме, а также в основе самой сути глаукомного поражения – формирования глаукомной экскавации ДЗН. Кроме того, активированные астроциты продуцируют синтаз оксида азота (NO) и тем самым секретируют NO, который легко диффундирует в окружающие ткани, включая аксоны. При одновременном усилении образования кислорода в аксонах создаются условия для синтеза достаточно агрессивной молекулы – пероксинитрита, который проникает через аксоны вглубь сетчатки, провоцируя гибель ганглиозных клеток сетчатки. А распространение пероксинитрита по направлению к мозгу приводит к потере клеток в наружных коленчатых телах. Глаукомное поражение является следствием умеренной, но рецидивирующей реперфузии (восстановление кровообращения после его снижения в результате колебаний офтальмотонуса), что ассоциируется с усилением окислительного стресса и повышением уровня свободных радикалов, в частности, супероксида. Наиболее ранние патологические изменения при глаукоме проявляются структурным повреждением митохондрий и гибелью клеток (Бездетко П.А., 2018).
Патологические явления усугубляются изменениями окружающих тканей, что вызвано активацией глиальных клеток, прежде всего астроцитов. Они начинают вырабатывать различные патологические субстанции, например, эндотелин, суживающий сосуды, а также матриксные металлопротеиназы, что приводит к исчезновению последнего и замещению его другим субстратом. Это явление получило название «ремоделирование тканей». Именно данный процесс лежит в основе изменений решетчатой мембраны склеры при глаукоме, а также в основе самой сути глаукомного поражения – формирования глаукомной экскавации ДЗН. Кроме того, активированные астроциты продуцируют синтаз оксида азота (NO) и тем самым секретируют NO, который легко диффундирует в окружающие ткани, включая аксоны. При одновременном усилении образования кислорода в аксонах создаются условия для синтеза достаточно агрессивной молекулы – пероксинитрита, который проникает через аксоны вглубь сетчатки, провоцируя гибель ганглиозных клеток сетчатки. А распространение пероксинитрита по направлению к мозгу приводит к потере клеток в наружных коленчатых телах. Глаукомное поражение является следствием умеренной, но рецидивирующей реперфузии (восстановление кровообращения после его снижения в результате колебаний офтальмотонуса), что ассоциируется с усилением окислительного стресса и повышением уровня свободных радикалов, в частности, супероксида. Наиболее ранние патологические изменения при глаукоме проявляются структурным повреждением митохондрий и гибелью клеток (Бездетко П.А., 2018).
Многие годы глаукома остается одной из главных причин слепоты в мире (European Glaucoma Society Terminology and Guidelines for Glaucoma, 2017).
В Украине доля инвалидизаций, обусловленных глаукомой, составляет около 20 %. Согласно официальной стаитистике, заболеваемость глаукомой в Украине за период с 2000-го по 2010 год возросла с 351 до 599 на 100 тыс. человек. Только за первое десятилетие XXI века заболеваемость глаукомой в нашей стране возросла на 41 % (Бездетко П.А., 2018).
Начальная стадия первичной открытоугольной глаукомы сложна для диагностики, поэтому наиболее часто диагноз первичной открытоугольной глаукомы ставится пациенту уже с развитой и далеко зашедшей стадиями заболевания (Еричев В.П., Дугина А.Е., Мазурова Ю.В., 2010), именно в этом и заключается коварство глаукомы. Компенсировать внутриглазное давление и стабилизировать зрительные функции на таких стадиях заболевания представляет довольно сложную задачу (Кондратенко Ю.Н., 2014, Клюєв Г.О., 2016).
Следовательно, основными критериями выбора препарата являются его эффективность и безопасность при длительном лечении. Выбор адекватной тактики ведения пациента позволяет значительно снизить риск дальнейшего прогрессирования глаукомы.
Согласно международных рекомендаций по лечению глаукомы European Glaucoma Society Terminology and Guidelines for Glaucoma, 4th Edition, 2017, препаратамипервойлиниивлеченииглаукомы являются простагландины (ПГ). Регулирующее влияние ПГ осуществляется через повышение или понижение активности рецепторов 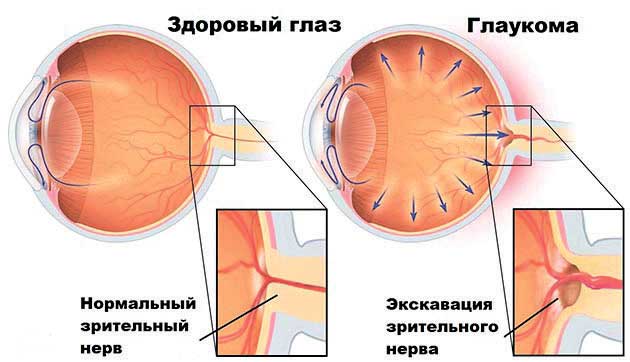 клеток, концентрации внутриклеточного медиатора цАМФ, кинетики кальция в клетке. За последнее время было выделено несколько типов простагландиновых рецепторов, специфичных для разных классов ПГ. В глазном яблоке человека наиболее часто встречается FP-тип рецепторов. Рецепторы этого типа локализуются в цилиарной мышце и эпителии, в трабекулярной ткани, в меланоцитах радужки и в эпителии капсулы хрусталика. Снижение офтальмотонуса при местном применении ПГ по данным A. Bill (1966) происходит вследствие усиления увеосклерального оттока водянистой влаги. По увеосклеральному пути оттекает около 20 % внутриглазной жидкости. Усиление увеосклерального оттока обусловлено взаимодействием со специфическими рецепторами, переходом неактивных матричных протеаз ресничной мышцы в активную форму, разрушением протеазами коллагеновых фибрилл экстрацеллюлярного матрикса, снижением толщины цилиарной мышцы и сопротивления оттоку водянистой влаги (Mishima H.K., et al., 1996). Аналоги простагландинов на сегодняшний день являются наиболее перспективным и разрабатываемым классом лекарственных препаратов.
клеток, концентрации внутриклеточного медиатора цАМФ, кинетики кальция в клетке. За последнее время было выделено несколько типов простагландиновых рецепторов, специфичных для разных классов ПГ. В глазном яблоке человека наиболее часто встречается FP-тип рецепторов. Рецепторы этого типа локализуются в цилиарной мышце и эпителии, в трабекулярной ткани, в меланоцитах радужки и в эпителии капсулы хрусталика. Снижение офтальмотонуса при местном применении ПГ по данным A. Bill (1966) происходит вследствие усиления увеосклерального оттока водянистой влаги. По увеосклеральному пути оттекает около 20 % внутриглазной жидкости. Усиление увеосклерального оттока обусловлено взаимодействием со специфическими рецепторами, переходом неактивных матричных протеаз ресничной мышцы в активную форму, разрушением протеазами коллагеновых фибрилл экстрацеллюлярного матрикса, снижением толщины цилиарной мышцы и сопротивления оттоку водянистой влаги (Mishima H.K., et al., 1996). Аналоги простагландинов на сегодняшний день являются наиболее перспективным и разрабатываемым классом лекарственных препаратов.
Одним из первых и наиболее известных представителей группы простагландинов является вещество Травопрост 0,004 % — синтетический простагландин F 2а, обладающий высокой селективностью по отношению к FP-рецепторам. Высокое сродство к рецепторам данного типа обеспечивает меньшую вероятность побочных эффектов (боль, гиперемия, жжение), которые реализуются посредством взаимодействия с другими простаноидными и непростаноидными рецепторами. Травопрост является липофильным пролекарством, преобразующимся в активную кислоту после прохождения через роговицу. Кислота травопроста взаимодействует с рецепторами цилиарной мышцы, клеток трабекулярной сети, вызывая разрушение экстрацеллюлярного матрикса и активируя увеосклеральный путь оттока. Применяется травопрост 1 раз в сутки вечером. Начальное снижение ВГД начинается через 2 часа после закапывания. Максимальное снижение ВГД достигается через 12 часов. Эффект сохраняется в течении 24 часов.
В ряде исследований (Миргородская С.А.,2008; Балалин С.В., Фокин В.П., 2017 ) доказано, что препараты травопроста, помимо снижения внутриглазного давления, обладают рядом дополнительных клинических эффектов, а именно:
- улучшение гемодинамики глаза, преимущественно, в задних цилиарных артериях на 12 %
- расширение поля зрения на 5–10 мм
- достоверное уменьшение относительных и абсолютных скотом
- уменьшение площади и объема экскавации зрительного нерва
- достоверное увеличение площади нейроретинального пояска диска зрительного нерва
- увеличение толщины слоя нервных волокон сетчатки по височному сектору
- увеличение суммарной светочувствительности сетчатки
- достоверное расширение периферического поля зрения
На отечественном фармакологическом рынке травопрост представлен глазными каплями ТРАВИНОР производства фармацевтической компании «Киевский витаминный завод». Данный препарат обладает всеми вышеизложенными свойствами травопроста, а также соответствует всем требованиям к препарату, снижающему внутриглазное давление, а именно:
- снижение внутриглазного давления в среднем до 30 % от исходного
- сохранение гипотензивного эффекта в течение 24 часов
- поддержание уровня внутриглазного давления с незначительными суточными колебаниями не более 5 мм.рт.ст.
- минимальное количество побочных эффектов
- удобный и простой режим инстилляций – 1 раз в сутки
- доступная и оправданная цена
Как было сказано, ТРАВИНОР относится к группе препаратов, направленных на улучшение оттока внутриглазной жидкости по трабекулярной сети и увеосклеральному пути. Однако в случаях, когда не представляется возможным снизить внутриглазное давление до необходимого уровня за счет использованя ТРАВИНОРА, в арсенале офтальмолога существует другая группа препаратов снижающих внутриглазное давление за счет уменьшения продукции водянистой влаги.
Известно, что при развитой стадии заболевания монотерапия в 40–75 % случаев не позволяет достичь оптимального уровня внутриглазного давления и стабилизации зрительных функций. В этом случае оправданным является назначение местных комбинированных гипотензивных препаратов (Куроедов А.В., 2007, Еричев В.П., 2008). В состав комбинированных офтальмологических препаратов с гипотензивным действием входят активные компоненты, терапевтический эффект которых усиливается при одновременном применении. Несомненным преимуществом комбинированной медикаментозной терапии является возможность отложить оперативное лечение с целью снижения уровня внутриглазного давления при развитой и далеко зашедшей стадиях глаукомы.
Рассмотрим более детально наиболее известную комбинацию гипотензивных препаратов, а именно, бета-блокаторов и ингибиторов карбоангидразы.
Бета-блокаторы, а именно тимолола малеат, относится к одной из наиболее часто встречающихся групп активных веществ, входящих в состав комбинированных препаратов с гипотензивным действием. Данный препарат начали применять в клинической практике еще с 60-х годов ХХ века. К преимуществам тимолола относятся высокая доступность для пациентов и эффективное снижение ВГД за счет снижения продукции водянистой влаги цилиарным телом. Однако для тимолола характерны недостатки, связанные с воздействием на сердечно-сосудистую и дыхательную системы. Тем не менее, тимолол чаще всего включают в фиксированные комбинации для лечения глаукомы. Ингибитор карбоангидразы дорзоламид, напротив, является относительно новым средством, которое применяют в терапии глаукомы около 20 лет. Препарат обладает достаточно высокой эффективностью в снижении внутриглазного давления (до 25–30 %) и блокирует выработку водянистой влаги (Бездетко П.А., 2018). Кроме эффективного снижения ВГД, дорзоламид также оказывает положительное действие на кровоток в области зрительного нерва, проявляет выраженные антиоксидантные и противоотечные свойства.
Фиксированная комбинация ингибитора карбоангидразы дорзоламида и тимолола малеата существует около 10 лет. Результаты клинических исследований свидетельствуют о ее эффективности и безопасности для лечения пациентов с первичной глаукомой различных стадий (Hutzelmann J., Owens S., Shedden A. et al. 1998; Bacharach J., Delgado M.F., Iwach A.G., 2003; He M., Wang W., Huang W., 2013; Cheng J.W., Cheng S.W. et al., 2013). Было также отмечено положительное влияние лечения данной комбинацией на гемодинамику глаза (Martinez A., Sanchez M. A., 2006; 2008). Недавно получены данные о способности фиксированной комбинации дорзоламида с тимололом усиливать перфузию капилляров сетчатки и диска зрительного нерва, а также о нарастании данного эффекта на фоне длительной терапии (Siesky B., Harris A., Kagemann L., 2010). В 2010 г. Siesky B. и соавт. установили, что при окислительном стрессе дорзоламид и тимолол способны предотвращать повреждение ДНК митохондрий клеток трабекулярного эндотелия (Saccа S.C., Pascotto A. et al. , 2005; Izzotti A, Sacc S.C., Di Marco B. et al., 2008; Miyamoto N., Izumi H., Miyamoto R. et al., 2009), а комбинация данных препаратов приводит к усилению антиоксидантного эффекта. Это позволяет воспрепятствовать повреждающему действию перекиси водорода на трабекулу (Sacca S., La Maestra S., Micale R., et al., 2011). Среднее снижение ВГД приназначениификсированнойкомбинациидостигает 30 % от исходного уровня. В сравнении с отдельным назначением дорзоламида и тимолола малеата статистически достоверное дополнительное снижение уровня внутриглазного давления достигается в 83 % случаев (Bacharach J., Delgado M.F., Iwach A.G., 2003).
ЭТО ВАЖНО!
Благодаря перечисленным эффектам применение тимолола в комбинации с дорзоламидом позволяет достичь комплексного воздействия на патогенетические механизмы глаукомы и более эффективно снижать внутриглазное давление по сравнению с монотерапией тимололом или дорзоламидом.
Первый отечественный комбинированный препарат, содержащий тимолола малеат и дорзоламид, представлен глазными каплями ДОРЗИТИМ производства фармацевтической компании «Киевский витаминный завод».
Основные фармакологические свойства и клинические эффекты ДОРЗИТИМА:
- отсутствие местных реакций в виде жжения и покраснения
- эффективен в отношении всех типов глауком (первичной, вторичной, псевдоэксфолиативной, неоваскулярной, травматической)
- каждый из компонентов препарата снижает внутриглазное давление за счет собственных механизмов действия
- отсутствие побочных эффектов в виде сужения зрачка, суженного поля зрения и ночной слепоты, характерных для препаратов пилокарпина
- снижает внутриглазное давление на 20–40 % от исходного в зависимости от стадии глаукомы, что соответствует международным критериям терапии глаукомы
- оказывает нейропротективное, антиоксидантное и положительное гемодинамическое действие на зрительный нерв и сетчатку
- удобная кратность применения до 2 раз в день, что поддерживает приверженность пациентов лечению
- доступная ценовая политика
ЭТО ВАЖНО!
ТРАВИНОР и ДОРЗИТИМ производятся из высококачественных субстанций (производства продукции in bulk «Рафарм С.А.», Греция). Система качества фармацевтической компании «Киевский витаминный завод» соответствует требованиям ДСТУ ISO 9001:2009 и международному стандарту ISO 9001:2008.
 Препараты ТРАВИНОР и ДОРЗИТИМ позволяют добиться стойкого снижения внутриглазного давления и поддерживать высокие зрительные функции на протяжении всего периода применения, как при монотерапии, так и при сочетанном применении данных капель.
Препараты ТРАВИНОР и ДОРЗИТИМ позволяют добиться стойкого снижения внутриглазного давления и поддерживать высокие зрительные функции на протяжении всего периода применения, как при монотерапии, так и при сочетанном применении данных капель.
Опираясь на проведенные клинические исследования (Сидорова М.В., 2018), важно отметить особенности применения капель ТРАВИНОР и ДОРЗИТИМ в зависимости от стадии глаукомы:
- у пациентов с І и ІІ стадией глаукомы монотерапия ТРАВИНОРОМ позволила добиться снижения показателей внутриглазного давления на 34,42 % от исходного.
- пациентам с ІІІ стадией глаукомы и исходным давлением выше 28 мм.рт.ст. целесообразно сразу назначать три действующих гипотензивных вещества, представленных в двух глазных формах ТРАВИНОР и ДОРЗИТИМ.
ГЛАЗНЫЕ КАПЛИ ТРАВИНОР И ДОРЗИТИМ – ЭТО ДОКАЗАННОЕ СОЧЕТАНИЕ
![]() Минакова Светлана врач-офтальмолог, канд. мед. наук ВМКЦ ГПСУ т. Одесса
Минакова Светлана врач-офтальмолог, канд. мед. наук ВМКЦ ГПСУ т. Одесса
 15-май-2026
15-май-2026