Пост-ковідні розлади здоров’я – пост-ковідний синдром: клінічний випадок практикуючого лікаря

ВСТУП. За останні півтора року світ і життя людей змінились. Світова спільнота зіткнулась з негаданим викликом — появою високо контагіозного та високо вірулентного нового коронавірусу SARS-CoV-2, що спричиняє гостре респіраторне захворювання COVID-19.
Статистика захворюваності та розповсюдження COVID-19 вражає. Важкий гострий респіраторний синдром нового коронавірусу (SARS-CoV-2) був виявлений в Китаї в грудні 2019 року. З тих пір понад 100 мільйонів людей у всьому світі були інфіковані та понад 2 мільйони людей померли від коронавірусної хвороби 2019 (COVID-19) [1]. Міжнародні фахівці прикладають зусилля для вирішення цієї проблеми і бачать за найкращу стратегію подолання пандемії — карантинні заходи та вакцинопрофілактику цього захворювання.
Однак багатьом людям вже довелось зіткнутися з цією хворобою або особисто, або у близьких та знайомих. І, окрім часто тяжкого перебігу хвороби, існують близькі та віддалені наслідки у людей, що перехворіли на COVID-19, які проявляються у розладах здоров’я та самопочуття [2]. Хоча безпрецедентні зусилля наукової та медичної спільноти були спрямовані на виявлення, діагностику, лікування та профілактику COVID-19, стійкі наслідки для людей після гострої фази захворювання ще не достатньо вивчені.
Наслідки COVID-19
Перенесений COVID-19 може спричиняти наслідки та медичні ускладнення, які тривають від декількох тижнів до декількох місяців після початкового одужання [3]. На сьогоднішній день не існує встановленої назви, яка би характеризувала персистуючий або стійкий стан у осіб з тривалими наслідками COVID-19. Різні автори використовують терміни «Long-COVID-19» (Довгий COVID-19), «Post-acute COVID-19» (Післягострий COVID-19), «Long-term COVID-19 effects» (Довготривалі ефекти COVID-19), «Post COVID-19 syndrome» (Синдром після COVID-19) та інші.
Симптоми, ознаки або ненормальні клінічні параметри, що зберігаються два та більше тижнів після COVID-19 і не повертаються до здорового вихідного рівня, потенційно можуть вважатися довготривалими наслідками захворювання. Незважаючи на те, що такі зміни в основному зустрічаються в осіб, які перенесли тяжку форму захворювання, стійкі наслідки також спостерігаються і в осіб з легкою інфекцією, які не потребували госпіталізації. Ще не встановлено, чи впливають суттєво стать, вік, етнічна приналежність, вихідний стан здоров’я, доза вірусу або прогресування COVID-19 на ризик розвитку довгострокових наслідків COVID-19 [4].
Серед проявів «пост-ковідного синдрому» є синдром хронічної втоми (СХВ), головний біль, довготривалий субфібрилітет, біль у суглобах (реактивний вірусний артрит), збільшення лімфатичних вузлів (лімфоаденопатія), порушення дихання (диспное, задишка), втрата смаку, пітливість, нудота, втрата волосся [5].
Після гострого епізоду SARS-CoV-2 у деяких пацієнтів розвивається синдром хронічної втоми, так званий міалгічний енцефаломієліт (CХВ/ME), який більш ніж 2–3 місяці після мікробіологічного одужання заважає їм повернутися до роботи та звичного образу життя [2–5]. Після подолання гострої інфекції COVID-19 у підгрупи пацієнтів, які перебувають на стадії реконвалесценції, можуть спостерігатися довгострокові побічні ефекти, що нагадують симптоматику CХВ/ME, такі як стійка втома, дифузна міалгія, депресивні симптоми та порушення сну. Дослідження показали, що вірус SARS-CoV-2 здатен проникати через гематоенцефалічний бар’єр до гіпоталамусу через нюхові шляхи [2, 6]. Ймовірний патогенез відповідає типовим ознакам у хворих на CХВ/ME, включаючи порушення лімфодренажу від мікроглії у головному мозку [3–7]. Один з основних шляхів лімфодренажу мозку проходить через периваскулярні простори уздовж нюхових нервів через ґратчасту кістку (os ethmoidale) до слизової оболонки носа [4, 8]. Якщо патогенез коронавірусу впливає на цей шлях, то це може пояснити аносмію, що спостерігається у частини хворих на COVID-19. Дані порушення призводять до накопичення прозапальних агентів, особливо постінфекційних цитокінів, таких як інтерферон-гамма та інтерлейкіни [5], які, як припускають, впливають на неврологічний контроль «глімфатичної системи» [3–6]. Накопичення цитокінів у центральній нервовій системі (ЦНС) може призвести до появи довготривалих симптомів вірусної інфекції. Прозапальні цитокіни потрапляють через гематоенцефалічний бар’єр у навколошлуночкові ділянки мозку, такі як гіпоталамус, що призводить до вегетативної дисфункції, яка у гострій фазі проявляється як висока температура тіла, а в довгостроковій перспективі веде до порушення регуляції циклів сон/неспання, когнітивної дисфункції та глибокої нестримної анергії і порушення терморегуляції (довготривалий субфібрилітет) [3, 4, 9].
Патогенез асоційованого з вірусом артриту зрозумілий лише частково, але одним із механізмів, який повинен опосередковувати активацію запального процесу, є молекулярна мімікрія [16], що відповідає за викликання автоімунних реакцій у схильних осіб [10, 11]. Повідомляються приклади молекулярної мімікрії щодо SARS-CoV-2 [12], і цей механізм гіпотетично бере участь у патогенезі як гострої системної інфекції, так і пост-інфекційних імунологічних наслідків, пов’язаних з вірусом [11, 12]. Попередні та фактичні дослідження демонструють, що коронавіруси діляться молекулярними епітопами з людськими білками (наприклад, глікопротеїном S-spike), які відіграють ключову роль у вторгненні до клітин-хазяїнів та уникненні від атак імунної відповіді, надаючи інфекційному агенту імуно-ухильну здатність [5, 8–13] . Відомо, що SARS-CoV2 поділяє три послідовності з шести амінокислот з такою кількістю людських білків у стовбурі мозку, і перехресна реакція між людськими та вірусними епітопами може призвести до пошкодження стовбура мозку та дихальної недостатності [14]. Інші ймовірні приклади подібних автоімунних запалень, зумовлених молекулярною мімікрією після COVID-19, відомі з публікацій, що повідомляють про випадки синдрому Гійєна-Барре та Міллера-Фішера [14, 15]. Імітуючі епітопи також можуть бути присутніми в синовіальній оболонці та викликати, за подібним механізмом, гостре місцеве запалення [16, 17].
Таким чином, після гострої фази захворювання у частини хворих на COVID-19 може продовжуватися розвиватися важкий поствірусний синдром — тривалий стан хронічної втоми, що характеризується нейроімунним виснаженням після значного інфекційного навантаження [8, 9, 14, 16].
КЛІНІЧНИЙ ВИПАДОК.
Пацієнтка N. 35 років без особливих супутніх захворювань захворіла на COVID-19 у середині серпня 2020 року, хворіла протягом 2 тижнів, перебіг середнє-тяжкий, лікувалась амбулаторно у Медичному центрі Х з діагнозом COVID-19, U07.1, вірусний пневмоніт поєднаний з двосторонньою нижньодольовою пневмонією, середнього ступеню тяжкості. Дихальна недостатність — 0 (ПЛР тест на SARS-CoV-2 позитивний у день звернення). Звернулась за медичною допомогою на 3-й день захворювання. При зверненні пацієнтка пред’являла скарги на загальну слабкість, рідкісний непродуктивний кашель, температуру 38,5о С. За період спостереження та лікування ЧДД 16-18 в хвилину, SpO2 атмосферним повітрям 97–98 %. Фібрильна температура (38о С–38,5о С) трималася протягом тижня, після чого лишилась на рівні стійкого субфібрилітету. Кашель у перші 4 дні сухий, з 5-ї доби мокрий. Відмічалося збільшення лімфатичних вузлів 3-х груп.
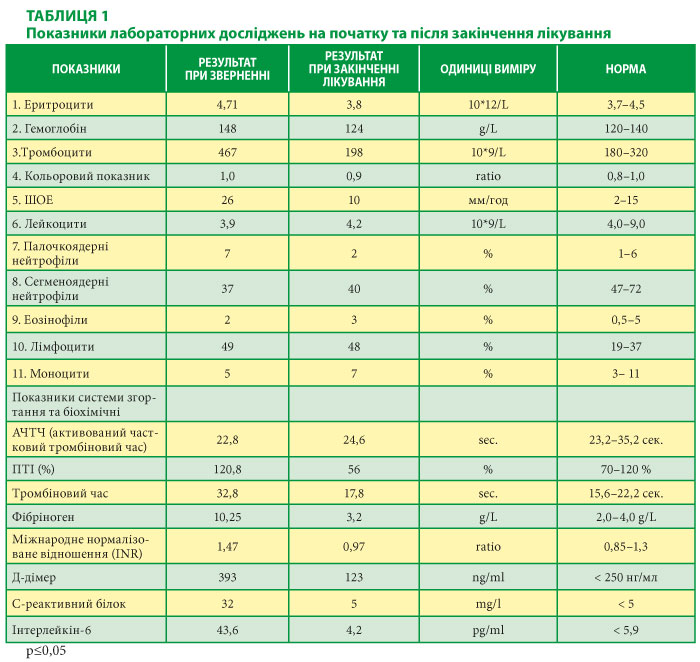
Лабораторні дослідження у перші 2 дні лікування:
- ПЛР тест на SARS-CoV-2 позитивний;
- КТ-легень — симптом матового скла, локальні ретикулярні зміни на тлі матового скла («crazy-paving» sign), по 2-х осередки ущільнення <3 см за діаметром у обох нижніх долях легень;
- клінічний аналіз крові: гемоглобін 148 г/л, тромбоцити 467*10^9, лейкоцити — 3,9*10^9, еозинофіли 2 %, палочкоядерні — 7 %, сегментоядерні — 37 %, моноцити — 5 %, лімфоцити — 49 %, ШОЕ 26 мм/год;
- коагулограмма: АЧТЧ (активований частковий тромбіновий час) 22,8 с, ПТІ 120,8 %, тромбіновий час 33,8 с, фібріноген 10,25 г/л, міжнародне нормалізоване відношення (INR) 1,47;
- Д-димер 393 нг/л;
- С-реактивний білок 32 мг/л;
- Інтерлейкін-6 –43,6 пг/л.
Було призначене лікування:
- противірусна терапія — Арбівір 200 мг 1 таб 2 рази на добу 5 днів;
- антибактеріальна терапія — Азітроміцин 500 мг
2 рази на день 3 дні без значної позитивної динаміки, з 4-го дня лікування Цефтріаксон 1 г 2 рази на день 5 днів, з 6-го дня Левофлоксацин 500 мг 2 рази на день ще 5 днів; - дексаметазон 4 мг в/м 2 рази на день 5 днів;
- антитромбатична терапія — клопридогрел 0,75 г
2 рази на день 5 днів і 10 днів 1 раз на добу; - симптоматична (ібупрофен 400 мг 2 рази на день 10 днів, віт. Д3 4000 ОД на добу 1 місяць, віт. С 500 мг на добу 1 місяць, цинк 125 мг на добу 1 місяць) та дезінтаксикаційна терапія і симптоматична терапія.
З 8-го дня лікування загальний стан пацієнтки нормалізувався, як і показники лабораторних досліджень. Однак у клінічному аналізі крові продовжувалися відзначатися низькі лейкоцити (4,2*10^9) та відносний лімфоцитоз (48 %) (Табл. 1). Також відзначалася субфібрильна температура тіла. Пацієнтка повторно була обстежена: ПЛР тест на SARS-CoV-2 негативний на 10-й день лікування. Виписана у задовільному стані.
Через 2 тижні після мікробіологічного одужання пацієнтка знов звернулась до клініки зі скаргами на головний біль, погану концентрацію уваги, панічні атаки, пов’язані з відчуттям тяжкого дихання, довготривалий субфібрилітет, збільшення лімфатичних вузлів 5 груп (заднєшийних, шийних, підщелепних, надключичних, пахвових лімфовузлів) при пальпації розміром від квасолини (заднєшийні, шийні, надключичні та пахові) до грецького горіху (підщелепні), болях у суглобах 4 груп (ліктьові, колінні, суглоби зап’ястні та пальців рук).
Після лабораторного обстеження були відмічені зміни у показниках (Табл. 2).
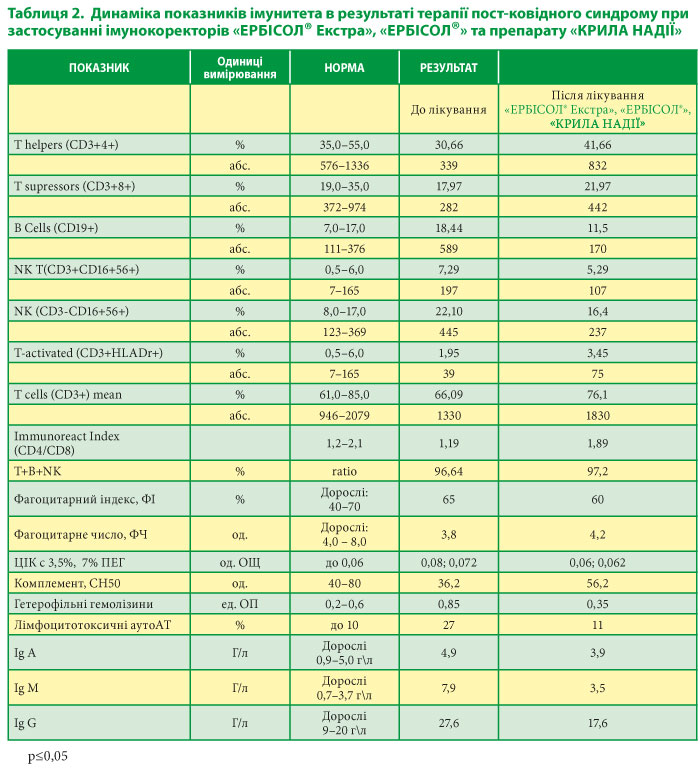
Діагностовано ознаки пост-ковідного синдрому, вторинна імунна дисфункція субкомпенсована, переважно за клітинною ланкою, реактивний артрит, легкий перебіг.
Лікувальна терапія базувалась на застосуванні ЕРБІСОЛОТЕРАПІЇ, комплексному використанні молекулярних імунокоректорів класу «ЕРБІСОЛ®»: «ЕРБІСОЛ® Екстра», «ЕРБІСОЛ®» та препарату «КРИЛА НАДІЇ» за схемою (Табл. 3).
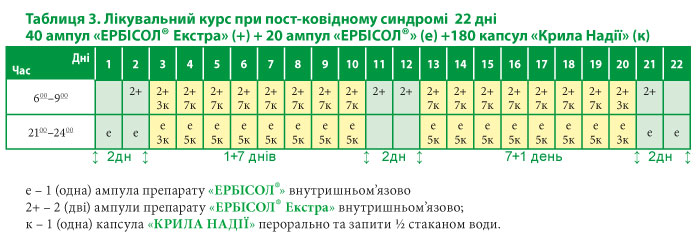
Згідно з рекомендаціями виробника ін’єкції препаратів робили на голодний шлунок, (за 1–2 год до їжі або через 2–3 год після їжі; чай, соки, воду, тощо можна було вживати). Капсули рекомендовано приймати з водою на голодний шлунок, за 30–40 хв перед ін’єкцією. Через 20–30 хв. після прийому капсул рекомендовано прийняти додатково пів стакану води та через 10 хв зробити ін’єкцію. Ввечері капсули призначалися через 3 год після вечері.
Додатково через день проводилася дезінтаксикаційна терапія (Реосорбілакт 400 мл) 10 маніпуляцій.
На 5-й день лікування скарги помітно зменшились (за умовною шкалою інтенсивності, де максимум — 10 балів, відсутність скарг — 0), то якщо прийняти сукупність вихідних скарг при повторному зверненні за 10 балів, то на 5 день лікування пацієнтка їх характеризувала на рівні 4 балів: субфібрилітет не відмічався, починаючи уже з 3 дня лікування, симптоми втоми, головні болі, порушення концентрації зменшувались поступово та відмічалися лише під час та після психофізичних навантажень і не дуже інтенсивно. Болі у суглобах зменшились, однак все ще відмічались. Лімфатичні вузли зменшились у розмірах, однак ще знаходились пальпаторно.
На 10-й день лікування позитивна динаміка продовжувалась: вихідні скарги на рівні 2–3 балів, температура стабільно нормалізувалась, симптоми втоми практично не відмічались пацієнткою, концентрація відновилася повністю, головні болі практично не відмічались за період з 5-го до 10-го дня лікування, біль у суглобах лишалась на тому ж рівні, лімфатичні вузли продовжували пальпуватись лише підщелепні та шийні розміром з квасолину.
Після закінчення лікування (на 25-й день) пацієнтка почувала себе задовільно, усі показники імунологічних досліджень прийшли до норми, скарги були відсутні. Були дані рекомендації про здоровий спосіб життя та призначена підтримуюча вітамінотерапія на 3 місяці.
РЕЗУЛЬТАТИ ТА ОБГОВОРЕННЯ

Наслідки COVID-19 ще недостатньо вивчені, однак все більше і більше повідомлень від науковців та практикуючих лікарів про випадки пост-ковідного синдрому, тому не дивлячись на те, що перед нами постає завдання докладного вивчення механізмів розвитку цього стану, вже зараз потрібні ефективні терапевтичні стратегії, що базуються на розумінні імунологічних механізмів пост-вірусного запалення. В такій ситуації ґрунтовно застосування відомих препаратів-імунокоректорів, що довго та широко використовуються при лікуванні подібних вторинних постінфекційних імунних та автоімунних розладів.
У якості такого засобу пацієнтці було призначено препарати «ЕРБІСОЛ® Екстра», «ЕРБІСОЛ®» та його пероральна форма «КРИЛА НАДІЇ», які вже більше 20 років застосовуються:
- у лікуванні імунних розладів;
- у комплексній терапії серцево-судинних та неврологічних захворювань, зокрема пов’язаних з порушенням мозкового кровообігу, поліневритів різного генезу, демієлізуючих полиневропатій;
- захворювань шлунково-кишкового тракту;
- неспецифічних захворювань легень, метаболічних дистрофій, ангіопатій, для покращання мікроциркуляції;
- захворювань сполучної тканини, системних васкулітів, артритів різної етіології.
Препарати мають виражені адаптивно-коригуючі властивості, підвищуючи компенсаторні та захисні функції організму та збільшуючи можливість фізичної активності та загального життєвого тонусу.
В даному лікувальному курсі препарати ряду «ЕРБІСОЛ®» були поєднані, так як комплексне застосування циклу даних імунокоректорів що доповнює один одне, створюючи єдину систему ЕРБІСОЛОТЕРАПІЇ.
Фармакологічна активність препаратів визначається вмістом у них біологічно активних пептидів, яким властиві імуномодулюючі, репаративні, антиоксидантні й антигіпоксичні ефекти.
Головний імуномодулюючий ефект даних препаратів проявляється, перш за все, через вплив на макрофагальну ланку імунної системи, яка відповідає за репарацію пошкоджених клітин та відновлення функціональної активності органів і тканин, а також через NК-клітини (CD3– 16+ 56+) і Т-кілери (CD3+ 16+ 56+), відповідальні за знищення пошкоджених клітин, нездатних до регенерації, або аномальних клітин. Одночасно препарати мають імунокоригуючу дію та при порушеннях імунного статусу сприяють його нормалізації внаслідок активації Т-лімфоцитів, Тh 1-хелперів і Т-кілерів, що важливо для відновлення балансу між клітинним та гуморальним імунітетом.
Важливим елементом фармакологічної активності препаратів «ЕРБІСОЛ® Екстра», «ЕРБІСОЛ®» та «КРИЛА НАДІЇ» є репаративні властивості, які обумовлюють процеси відновлення клітин та функціональної активності органів і тканин завдяки знищенню ушкоджених клітин, нездатних до регенерації.
ЕРБІСОЛОТЕРАПІЯ має антиоксидантний ефект, що проявляється за рахунок гальмування процесів перекисного окиснення ліпідів, підвищення активності глютатіон залежної антиоксидантної системи крові, без змін активності ферментів мікросомального окиснення та вмісту цитохрому Р450, а також мембрано-стабілізуючого ефекту на рівні плазматичних мембран.
Антигіпоксичні властивості «ЕРБІСОЛ® Екстра», «ЕРБІСОЛ®» та «КРИЛА НАДІЇ» реалізуються за рахунок підвищення споживання кисню тканинами та поліпшення клітинного дихання у результаті посилення транспорту електронів у мітохондріях, а також підсиленню віддачі кисню тканинам.
Препарати нетоксичні та позбавлені кумулятивної токсичності, алергенних, тератогенних, мутагенних і канцерогенних властивостей.
Широкий досвід у використанні даних препаратів при лікуванні імунних порушень, неврологічних розладів та реактивних артритів був аргументом для визначення стратегії лікування даної пацієнтки.
Швидкий прогрес стану хворої в результаті застосування імунокорегуючих препаратів ЕРБІСОЛОТЕРАПІЇ дозволяє рекомендувати їх використання у випадках пост-інфекційних наслідків взагалі та зокрема при терапії пост-ковідного синдрому, ґрунтуючись на фармакологічних ефектах, націлених на відновлення та репарацію організму завдяки реалізації механізмів ефективного завершення запального процесу, що дозволяє поновити функціонування органів і систем й очистити їх від уражених, дефектних та недієздатних клітин. Детоксикація на молекулярному рівні прискорює та нормалізує метаболічні внутріклітинні процеси оновлення, а інтенсифікація тканинного дихання дозволяє позбавитися від агресивного впливу вільних радикалів.
Характерною особливістю імуномодулюючої активності препаратів класу «ЕРБІСОЛ®» є активація ними клітин як макрофагального, так і кілерного ряду.
Імуномодулююча активність препарату «ЕРБІСОЛ® Екстра» спрямована здебільше (65–85 %) на активізацію макрофагів М2А (протизапального) фенотипу, що запускають процеси репарації пошкоджених клітин і регенерацію тканин, а також відновлення функціонального стану органів і тільки (15–35 %) активність препарату спрямована на активацію кілерної ланки імунного захисту [18].
Препарат «ЕРБІСОЛ®» активує репаративну та кілерну ланку в рівній мірі, поєднуючи їх в допустимих пропорціях універсального препарату.
Препарат «КРИЛА НАДІЇ» є проміжнім продуктом виробництва препаратів класу «ЕРБІСОЛ®» та біологічно активною добавкою і ефективно посилює дію препаратів «ЕРБІСОЛ®» та є важливою частиною ЕРБІСОЛОТРАПІЇ.
У класі цього типу препаратів існує ще один вид імунокоректора «ЕРБІСОЛ® УЛЬТРАфарм». Його імуномодулююча активність перш за все (на 70–80 %) націлена на активізацію кілерної ланки, відповідальної за знищення пошкоджених клітин, нездатних до регенерації, або аномальних клітин (мутантних, злоякісних, клiтин-вірусоносіїв тощо) і нежиттєздатних ділянок тканин, а також для лікування захворювань вірусної та мікробної етіології. Саме ці властивості роблять його використання доцільним та найбільш обґрунтованим в гострій фазі захворювання на COVID-19, однак це потребує подальших досліджень.
ВИСНОВКИ
Новий коронавірус SARS-CoV-2 значно вплинув на світове суспільство і важко прогнозувати остаточні наслідки пандемії, однак вже очевидні численні розлади здоров’я людей, причиною яких є COVID-19. Подальші дослідження особливостей взаємодії вірусу та організму людини — це справа майбутнього, але вже зараз багато пацієнтів потребують зваженої та раціональної допомоги для подолання цього захворювання та його наслідків. Використовуючи підходи світової медичної спільноти з пошуку фармакологічних речовин для лікування COVID-19 із спектру вже відомих препаратів з гарно вивченою ефективністю, механізмом дії та профілем безпеки за мети надати необхідну допомогу хворим на COVID-19 та пацієнтам з його наслідками — пост-ковідним синдромом, можна рекомендувати у якості можливої терапевтичної стратегії ЕРБІСОЛОТЕРАПІЇ, що включає комплекс лікування препаратами класу «ЕРБІСОЛ®»: «ЕРБІСОЛ® Екстра», «ЕРБІСОЛ®» та «КРИЛА НАДІЇ».
Література:
- Hannah Ritchie EO-O, Diana Beltekian, Edouard Mathieu, Joe Hasell, Bobbie Macdonald, Charlie Giattino, and Max Roser // Coronavirus Pandemic (COVID-19). 2021. [Google Scholar]
- Tenforde MW, Kim SS, Lindsell CJ, [et al.] Symptom Duration and Risk Factors for Delayed Return to Usual Health Among Outpatients with COVID-19 in a Multistate Health Care Systems Network — United States, March-June 2020 // MMWR Morb Mortal Wkly Rep 2020; 69(30): 993–8. [PMC free article] [PubMed] [Google Scholar]
- Townsend L, Dowds J, O’Brien K, [et al.] Persistent Poor Health Post-COVID-19 Is Not Associated with Respiratory Complications or Initial Disease Severity // Ann Am Thorac Soc 2021. [PubMed] [Google Scholar]
- Gemelli Against C-P-ACSG. Post-COVID-19 global health strategies: the need for an interdisciplinary approach // Aging Clin Exp Res 2020; 32(8): 1613–20. [PMC free article] [PubMed] [Google Scholar]
- Greenhalgh T, Knight M, A’Court C, Buxton M, Husain L. Management of post-acute covid-19 in primary care // BMJ 2020; 370: m3026. [PubMed] [Google Scholar]
- Chen Q, Allot A, Lu Z. LitCovid: an open database of COVID-19 literature // Nucleic Acids Res 2021; 49(D1): D1534–D40. [PMC free article] [PubMed] [Google Scholar]
- Xiong Q, Xu M, Li J, et al. Clinical sequelae of COVID-19 survivors in Wuhan, China: a single-centre longitudinal study // Clin Microbiol Infect 2021; 27(1): 89–95. [PMC free article] [PubMed] [Google Scholar]
- Goertz YMJ, Van Herck M, Delbressine JM, [et al.]. Persistent symptoms 3 months after a SARS-CoV-2 infection: the post-COVID-19 syndrome? ERJ Open Res 2020; 6(4). [PMC free article] [PubMed] [Google Scholar]
- Carfi A, Bernabei R, Landi F, Gemelli Against C-P-ACSG. Persistent Symptoms in Patients After Acute COVID-19 // JAMA 2020; 324(6): 603–5. [PMC free article] [PubMed] [Google Scholar]
- Townsend L, Dyer AH, Jones K, [et al.]. Persistent fatigue following SARS-CoV-2 infection is common and independent of severity of initial infection // PLoS One 2020; 15(11): e0240784. [PMC free article] [PubMed] [Google Scholar]
- Neufeld KJ, Leoutsakos JS, Yan H, [et al.]. Fatigue Symptoms During the First Year Following ARDS // Chest 2020; 158(3): 999–1007. [PMC free article] [PubMed] [Google Scholar]
- Wostyn P. COVID-19 and chronic fatigue syndrome: Is the worst yet to come? // Med Hypotheses 2021; 146: 110469. [PMC free article] [PubMed] [Google Scholar]
- Vink M, Vink-Niese A. Could Cognitive Behavioural Therapy Be an Effective Treatment for Long COVID and Post COVID-19 Fatigue Syndrome? Lessons from the Qure Study for Q-Fever Fatigue Syndrome // Healthcare (Basel) 2020; 8(4). [PMC free article] [PubMed] [Google Scholar]
- Gasparotto M, Framba V, Piovella C, [et al.] Post-COVID-19 arthritis: a case report and literature review // Clin Rheumatol. 2021 Feb 15:1-6. doi: 10.1007/s10067-020-05550-1 [PMC free article] [PubMed] [Google Scholar]
- Lamprecht B. Is there a post-COVID syndrome? // Pneumologe (Berl). 2020 Oct 8:1-4. doi: 10.1007/s10405-020-00347-0 [PMC free article] [PubMed] [Google Scholar]
- Perrin R, Riste L, Hann M, [et al.] Into the looking glass: Post-viral syndrome post COVID-19 // Med Hypotheses. 2020 Nov;144:110055. doi: 10.1016/j.mehy.2020.110055. Epub 2020 Jun 27. [PMC free article] [PubMed] [Google Scholar]
- Garg P, Arora U, Kumar A, [et al.] The «post-COVID» syndrome: How deep is the damage? // J Med Virol. 2021 Feb;93(2):673-674. doi: 10.1002/jmv.26465. Epub 2020 Sep 29. [PMC free article] [PubMed] [Google Scholar]
- Николаенко А.Н., Базыка Д.А., Дранник Г.Н. и др. Влияние препаратов класса Эрбисол на продукцию цитокинов и экспрессию поверхностных маркеров клеток крови у здоровых доноров и онкологических пациентов // Евразийский онкологический журнал. — 2016. — Т. 4, № 1. — С. 79–89.
![]() Тетяна Давидова, кандидат медичних наук,
Тетяна Давидова, кандидат медичних наук,
імунолог, старший науковий співробітник
лабораторії імунореабілітології ДУ «Інститут мікробіології
та імунології ім. І.І. Мечникова Національної академії
медичних наук України»

 12-май-2026
12-май-2026
